膜/跨膜蛋白抽提试剂盒
¥5062
推荐产品
公司新闻/正文
去垢剂如何帮助膜蛋白增溶?
4462 人阅读发布时间:2023-11-14 10:43
什么是去垢剂?
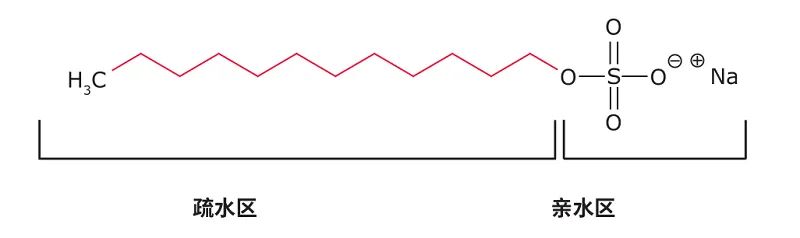
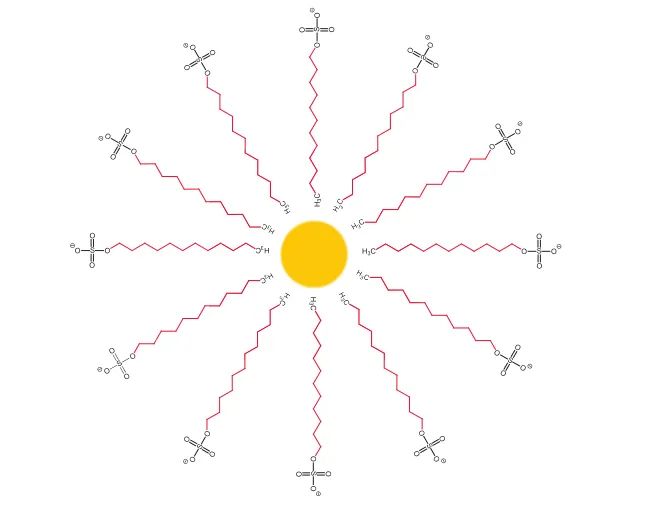
去垢剂是一种两亲性分子,在油性长烃基基团的末端(尾部)带有极性或带电荷的亲水性基团(头部)(图1)。该物质也被称为表面活性剂,因为其可以降低水的表面张力。与纯极性或非极性分子相反,两亲性分子会在水性介质中表现出一种独特的性质。此类分子的极性基团会与水分子结合形成氢键,而烃链会由于疏水相互作用而聚集在一起。在低浓度下,去垢剂以单体形式存在于水中。如果浓度达到某个值,该值被称为临界胶束浓度 (CMC),单体分子将形成一种被称为胶束的非共价聚集体。1-3 在胶束中,每个去垢剂分子的极性亲水部分都朝向极性溶剂(水),而碳氢化合物部分会形成一个在热力学上稳定的疏水核。胶束的简单图示(图2),展示了朝向这个概念。实际的胶束结构会更加复杂,整个结构会处于动态变化状态中,同时因去垢剂浓度和溶液成分的变化而发生变化。4图1. 阴离子去垢剂十二烷基硫酸钠 (SDS) 的结构,亲水和疏水区域请参见标识
图2. SDS 胶束的简单图示
去垢剂如何帮助膜蛋白增溶?
去垢剂广泛应用于生物化学、细胞生物学和分子生物学。常见应用包括细胞裂解、膜蛋白和脂质增溶、蛋白质结晶,以及减少印迹实验中的背景染色。 尽管膜蛋白研究是蛋白质生物化学所面临的一个重大挑战,但鉴于其重要的生物学和药理学相关性,该研究领域影响深远。要了解膜蛋白的结构和功能,就要在高纯化的状态下将其以天然形式慎重地分离出来。由于能够形成胶束的去垢剂提供了可以模拟脂质双层的两亲环境,因此将其用作增溶剂对于功能和结构研究而言至关重要。
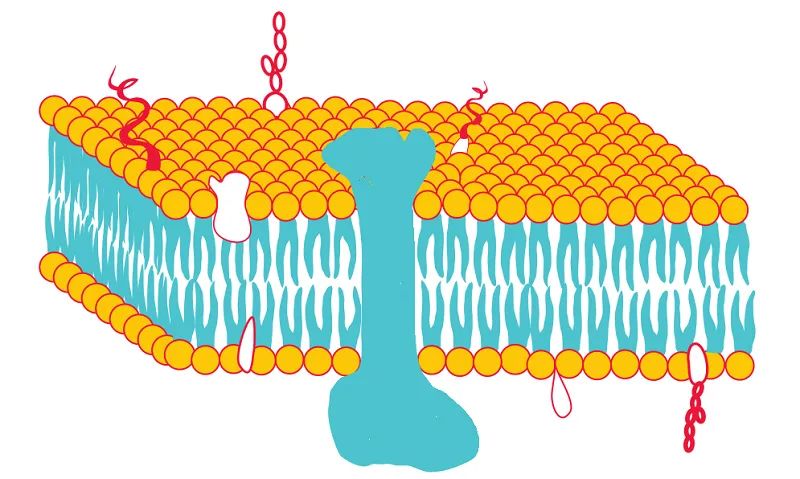
生物膜由磷脂组成,磷脂含有两个与极性头部基团相连的疏水基团。此分子结构使得磷脂可以组装成一种脂质双层结构,每一层的疏水链两两相连,各自的极性头部基团向外,暴露在水介质(图3)。蛋白质和脂质可以嵌入到该双层结构中,形成一种流体镶嵌模型(图4),该模型Singer和Nicolson于1972年首次提出。蛋白质通过脂质尾部和疏水蛋白结构域之间的疏水相互作用嵌在脂质双层中。5 内在膜蛋白 (IMP)(图4)不溶于水溶液,其会聚集在一起以保护其疏水域,但可溶于去垢剂溶液——因为去垢剂形成的胶束类似于生物膜的双层结构。6 蛋白质通过疏水相互作用嵌在这些胶束中。以前嵌在膜脂双层中的膜蛋白的疏水区域现在被一层去垢剂分子包围,而亲水区域暴露在水介质中。这使得膜蛋白可以以溶液形式存在。完全除去去垢剂可能会导致膜蛋白由于疏水区域的聚集而发生集聚,以至于出现沉淀。图3. 磷脂双层
去垢剂对膜的增溶作用可视为一个三步过程,其中去垢剂-脂质-蛋白质比是一个重要参数(图5)。图4. 生物膜的流体镶嵌模型
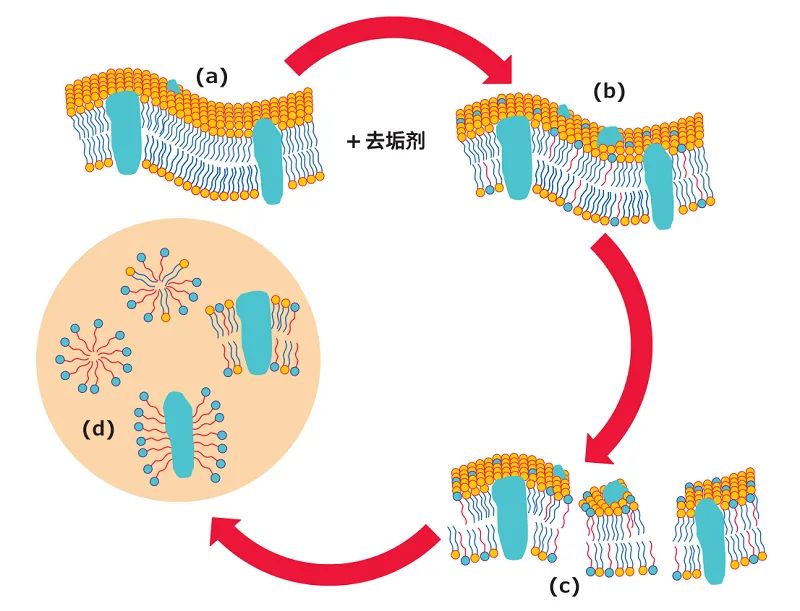
图5. 去垢剂的生物膜增溶过程。当将低浓度的去垢剂添加到生物膜 (a) 时,去垢剂单体(以红色显示,带有单尾)通过进入到脂质双层 (b) 来打乱膜的结构。在等于或高于去垢剂的CMC的浓度下,脂质双层中的去垢剂分子达到饱和状态,随即分裂生成脂质-蛋白质-去垢剂混合胶束 (c)。8 在去垢剂/蛋白质的比值达到1-2 (w/w) 时,其可以溶解IMP,形成脂质-蛋白质-去垢剂混合胶束。9去垢剂浓度的进一步升高会导致脂质-蛋白质-去垢剂混合胶束逐渐脱脂,形成脂质/去垢剂和蛋白质/去垢剂混合胶束 (d)。8 增溶IMP与结合去垢剂的复合物被称为蛋白质-去垢剂复合物。10 一般来说,10 (w/w) 或更高的去垢剂/蛋白质比值会导致完全脱脂。11
去垢剂的分类
根据其结构的不同,去垢剂大致可分为:12- 离子型去垢剂
- 非离子去垢剂
- 两性离子去垢剂
离子型去垢剂
离子去垢剂中含有阴离子或阳离子头部基团,其带有净电荷。疏水性尾部要么是直链烃链,如SDS 和CTAB,要么是刚性甾体基团,如胆汁酸盐。13 离子去垢剂胶束的大小由以下因素的综合作用决定:侧链的疏水吸引力和离子基团的排斥力。因此,随着反离子浓度的增加,头部基团上的电荷会被中和,导致胶束尺寸变大。同时,胶束大小也会随着烷基链长度的增加而增加。离子去垢剂在膜蛋白增溶方面非常有效,但同时,也几乎总是会在一定程度上导致蛋白变性。6阴离子去垢剂 Sigma-Aldrich®推荐

阳离子去垢剂 Sigma-Aldrich®推荐
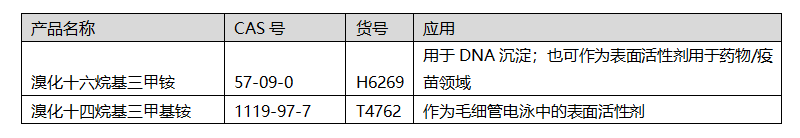
非离子去垢剂
非离子去垢剂含有不带电荷的亲水性头部基团,如BRIJ® 和TRITON™去垢剂,也可以是糖苷基团,如辛基葡萄糖苷和十二烷基麦芽糖苷。由于非离子去垢剂会破坏脂质-脂质和脂质-蛋白质,但不会破坏蛋白质-蛋白质相互作用,因此其属于非变性去垢剂。14 因此,其在具有生物活性形式的膜蛋白分离过程中得到了广泛应用。与离子去垢剂不同,盐类对非离子去垢剂的胶束大小的影响很小。6 非离子去垢剂 Sigma-Aldrich®推荐
两性离子去垢剂
两性离子去垢剂兼有离子型和非离子型的特点。与非离子去垢剂一样,两性去垢剂不带净电荷,不具有导电性和电泳迁移率,不会与离子交换树脂结合。然而,与离子去垢剂一样,其可以有效地破坏蛋白质-蛋白质相互作用。基于类固醇的两性去垢剂,如CHAPS,相比于直链两性离子去垢剂(例如,十二烷基二甲基二胺氧化物)所导致的变性更少。15 两性离子去垢剂 Sigma-Aldrich®推荐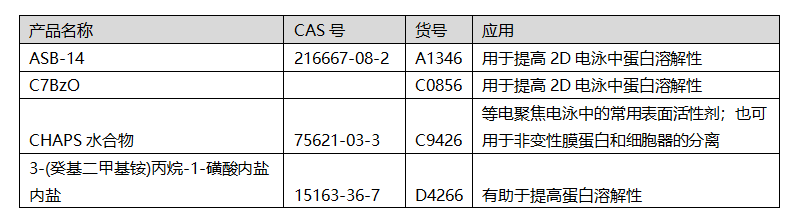
默克Sigma-Aldrich®去垢剂优势
默克Sigma-Aldrich® 去垢剂和表面活性剂系列的产品化学稳定性好,满足了从适用于普通实验室的试剂级别到适用最苛刻应用的高纯度级别等各级需求。支持ISO 90001:2008认证产品批量和定制生产,既能满足实验室小规模产量需求,也能进行大规模批量生产。
文献参考: 1. Linke, D. (2009) Methods Enzymol. 463, 603–617. 2. Arnold, T. and Linke, D. (2008) Curr. Protoc. Protein Sci. 53:4.8:4.8.1–4.8.30. 3. Arnold, T. and Linke, D. (2007) Biotechniques. 43, 427-434. 4. Garavito, R. M. and Ferguson-Miller, S. (2001) J. Biol. Chem. 276(35), 32403-32406. 5. Singer, S. J. and Nicolson, G. L. (1972) Science. 175(4023), 720-31. 6. Seddon, A. M., et.al. (2004) Biochim. Biophys. Acta. 1666(1-2), 105-117. 7. Rosen, M. (2004) Surfactants and Interfacial Phenomena. 3rd ed. John Wiley & Sons, Inc., Hoboken, NJ. 8. Kalipatnapu, S. and Chattopadhyay, A. (2005) IUBMB Life. 57(7), 505 -512. 9. Lin, S.H. and Guidotti, G. (2009) Methods Enzymol. 463, 619-629. 10. Prive, G.G. (2009) Curr. Opin. Struct. Biol. 19, 379-385. 11. Hjelmeland, L.M. (1990) Methods Enzymol. 182, 253-264. 12. Neugebauer, J. M. (1990) Methods Enzymol. 182, 239-253. 13. Lórenz-Fonfría, V., et.al. (2011) Solubilization, Purification, and Characterization of Integral Membrane Proteins, in Production of Membrane Proteins: Strategies for Expression and Isolation. 1st ed. Wiley-VCH Verlag GmbH & Co. KGaA, Weinheim, Germany. 14. le Maire, M., et al. (2000) Biochim. Biophys. Acta. 1508(1-2), 86-111. 15. Lund, S., et al. (1989) J. Biol. Chem. 264(9), 4907-4915.